Propósitos
Analizar el comportamiento delos atomos de los elementos químicos cuando éstos se combinan.
Un enlace químico corresponde a la fuerza que une o enlaza a dos átomos, sean estos iguales o distintos. Los enlaces se pueden clasificar en tres grupos principales:
- Enlaces iónicos
- Enlaces covalentes
- Enlaces dativos.
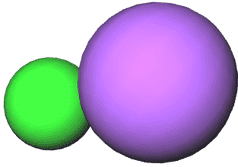
Enlace iónico: Un enlace iónico se puede definir como la fuerza que une a dos átomos a partir de que un elemento electropositivo se une con un elemento electronegativo. Mientras mayor sea la diferencia de electronegatividad entre los elementos, más fuerte será el enlace iónico. Se empieza a considerar que dos átomos están unidos a través de un enlace iónico cuando su diferencia de electronegatividad es superior a 1.7.
Enlace Covalente
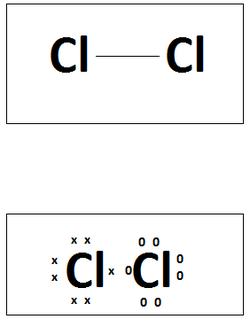
El enlace covalente es la fuerza que une dos átomos mediante la compartición de un electrón por átomo. Dentro de este tipo de enlace podemos encontrar dos tipos:
El enlace covalente polar:
Corresponde a todos aquellos compuestos en donde la diferencia de electronegatividad de los átomos que lo componen va desde 0 hasta 1.7 (sin considerar el 0)
Enlace covalente no polar:
Los compuestos que son no polares se caracterizan por ser asimétricos, tener un momento dipolar son solubles en agua y otros solventes polares, entre otras características.
El enlace covalente es la fuerza que une dos átomos mediante la compartición de un electrón por átomo. Dentro de este tipo de enlace podemos encontrar dos tipos:
El enlace covalente polar:
Corresponde a todos aquellos compuestos en donde la diferencia de electronegatividad de los átomos que lo componen va desde 0 hasta 1.7 (sin considerar el 0)
Enlace covalente no polar:
Los compuestos que son no polares se caracterizan por ser asimétricos, tener un momento dipolar son solubles en agua y otros solventes polares, entre otras características.
Actividades
¿Qué debo hacer?
- Elabora un mapa conceptual con las palabras claves del tema.
- Observa el vídeo, luego elabora una molécula de agua utilizando bolas de colores.
- Calcula la electronegatividad del agua.


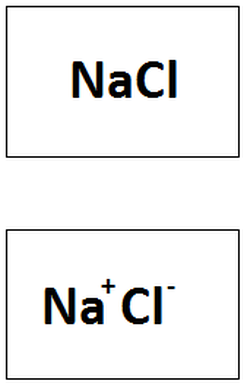
No hay comentarios.:
Publicar un comentario
Participa en este blog con tu cuenta Google (gmail). Debes elaborar una pregunta relacionada con el tema (hasta 10 puntos) o responder alguna elaborada por tus compañeros (hasta 5 puntos). El puntaje se asigna por orden de llegada.